2025年6月CDE发布了《中国新药注册临床试验进展年度报告(2024年)》,公布了2024 年药物临床试验登记与信息公示平台登记临床试验总量达 4900 项(以 CTR 计),较 2023 年增长了 13.9%。其中,新药临床试验(以受理号登记)数量为 2539 项,较 2023年增长了 9.3%。2024 年细胞和基因治疗类产品共登记临床试验 115 项,较 2023 年增加了 42.0%,以抗肿瘤适应症药物为主。
细胞和基因治疗品种及其临床试验
2024年细胞和基因治疗类药物新增首次登记临床试验115项(以CTR计),较2023年增加了42.0%(115 vs.81)。上述115项试验共涉及100个品种(以药品名称计),其中细胞治疗类62个品种,基因治疗类38个品种,适应症以抗肿瘤为主(50项,43.5%)。
从临床试验数量分析,细胞治疗类62个品种共登记临床试验75项,占比为65.2%(75/115);基因治疗类38个品种共登记临床试验40项,占比为34.8%(40/115)。临床试验项目数量占比较高的依次为干细胞类29项(25.2%)、CAR-T类27项(23.5%)、溶瘤病毒类8项(7.0%)和肿瘤浸润淋巴细胞(TIL)类 6项(5.2%)。
从试验分期分析,细胞和基因治疗类药物临床试验以Ⅰ期临床试验为主,共登记65项,占比为56.5%(65/115);Ⅱ期试验11项,占比为9.6%;Ⅲ期临床试验6项,占比仅为5.2%;其他试验33项,占比为28.7%。
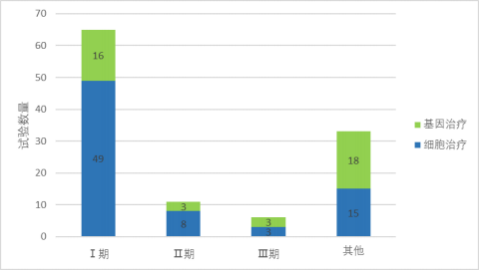
2024 年细胞和基因治疗类药物临床试验
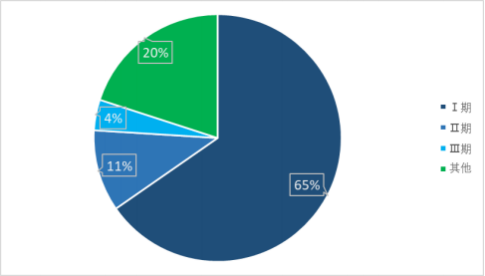
2024 年细胞治疗类药物临床试验分期占比
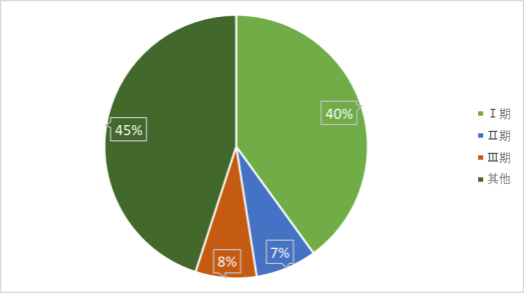
2024 年基因治疗类药物临床试验分期占比
从适应症分类分析,细胞治疗类 75 项临床试验抗肿瘤为38项,占比50.7%,其次为血液系统疾病9项(12.0%)。基因治疗类40项临床试验抗肿瘤为12项,占比30.0%,其次为皮肤及五官科9项,占比22.5%,神经系统疾病8项,占比20.0%。
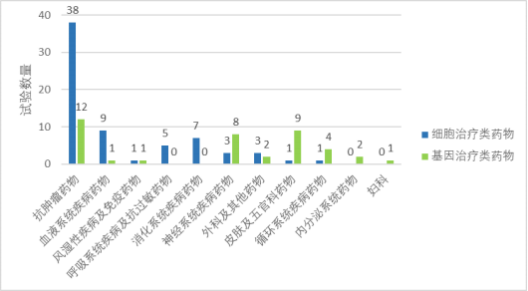
2024 年细胞和基因治疗类药物临床试验
对2024年新增首次登记占比较高的29项干细胞类临床试验进一步分析:
(1)从试验分期分析,Ⅰ期临床试验15项(51.7%)、Ⅱ期临床试验3项(10.3%)、Ⅲ期临床试验2项(6.9%)、其他类型试验9项(31.0%)。
(2)从细胞来源分析,间充质干细胞21项(72.4%)、造血干细胞5项(17.2%)、多功能分化干细胞1项(3.4%)、其他来源干细胞2项(6.9%)。
(3)从适应症分析,干细胞类临床试验均为非肿瘤适应症,占比较高的依次为血液系统疾病7项( 24.1%)、消化系统疾病6项(20.7%)、呼吸系统疾病5项(17.2%)。
